![]()
![]()
![]()
Use LEFT and RIGHT arrow keys to navigate between flashcards;
Use UP and DOWN arrow keys to flip the card;
H to show hint;
A reads text to speech;
100 Cards in this Set
- Front
- Back
- 3rd side (hint)
|
1-1. 0.5M H2SO4 50mL와 2M H2SO4 80mL 혼액에 물 몇 mL를 가하면 1M H2SO4가 되는가? |
답 : 55mL • 몰수(n) = 몰농도(M1)×부피(V1) + 몰농도(M2)×부피(V2) = 0.5mmol/mL×50mL + 2mmol/mL×80mL = 185mmol • 목표 부피(V3) = 몰수(n) / 몰농도(M3) = 185mmol / (1mmol/mL) = 185mL • 더해야 하는 부피 = 185mL - (50mL+80mL) = 55mL |
|
|
|
1-2. ☆ 활동도계수 (activity of coefficient, γ) |

(○) 이온세기가 증가하면 활동도계수는 감소한다. (○) 이온의 전하가 증가할수록 활동도계수는 감소한다. (○) 전하를 가지지 않는 중성분자의 활동도계수는 1이다. (×) 이온의 전하수가 같은 경우 수화반경이 클수록 활동도계수는 감소한다. |
화학종 a의 활동도(Aa) = a의 몰농도[a] × a의 활동도계수(γa) |
|
|
1-3. 해리상수가 1.6×10^-4인 약산 HA 0.1M 용액의 전리도는? |
답 : 4×10^-2 • 전리도(α) = [A-] / ([HA]+[A-]) [A-] ≪ [HA], [HA]+[A-]≒[HA], α≒[A-] / [HA] [A-]≒α[HA] • 해리상수(Ka) = [A-][H+] / [HA] = 1.6×10^-4 [HA]=0.1M, [A-]=[H+]≒α[HA], Ka≒α[HA]α[HA] / [HA] • 약산의 전리도 α ≒ √(Ka/[HA]) = √(1.6×10^-4/0.1) = 4×10^-2 |
|
|
|
1-4. 다음 화합물의 0.1M 수용액 중 전리도가 작은 순서 |
HCN (Ka = 1.0×10^-10) ∧ H3BO3 (Ka = 5.5×10^-10) ∧ NH4OH (Kb = 1.8×10^-5 ⇒ Ka = 5.6×10-^10) ∧ HAc (Ka = 1.8×10^-5) ∧ HCOOH (Ka = 1.8×10^-4) |
약산의 전리도 α ≒ √(Ka/[HA]) 약산의 전리도 α ∝ √Ka Ka × Kb = 10^-14 Ka = 10^-14 / Kb 문제에서 몰농도가 0.1로 동일하므로 해리성수Ka만 비교하면 풀수 있다. 전리도는 Ka의 제곱근에 비례 |
|
|
1-5. 반응식에서 짝산과 짝염기 NH3 + H2O ↔ OH- + NH4+ |
(○) H2O/OH- (×) NH3/OH- (○) NH3/NH4+ (×) OH-/NH4+ |
Bröensted-Lowry의 산 염기 |
|
|
1-6. 진한황산(98%, 비중=1.8)을 물에 사용하여 20배 희석한 용액의 농도는? 단, 황산의 분자량=98 |
답 : 0.9M • 원액부피=1000mL, 비중=1.8, 백분율=98%, 분자량=98 • 몰농도(M) = 몰수(n) / 1L = 질량(m) ÷ 분자량(MW) / 1L = 원액질량(m원액)×백분율(pc) ÷ 분자량(MW) / 1L = 원액부피(V)×비중(SG)×백분율(pc) ÷ 분자량(MW) / 1L = 1000mL원액×1.8g원액/mL원액×(98g황산/100g원액) ÷ 98g황산/mol / 1L = 18mol/L • 18mol/L를 20배 희석 ⇒ 18/20 = 0.9mol/L |
|
|
|
1-7. ☆ 전리도 (degree of ionization, α ) |
(○) 전해질의 전리도가 크면, 같은 몰농도의 비전해질에 비해 어는점 내림이 커진다. (×) 약산의 전리도는 그 수용액의 농도에 비례하여 증가한다. (×) 전리도는 물질의 고유한 특성으로 온도가 일정하면 농도에 상관없이 일정하다. (×) 약산의 전리도는 온도와 상관없이 주어진 농도에서는 일정하다. (×) 약염기의 전리도는 전기전도도와는 상관없다. |
• 전리도(α) = [A-] / ([HA]+[A-]) • 해리상수(Ka) = [A-][H+] / [HA] • 산의 전리도 α ∝ 1/[HA] 산의 전리도는 산의 농도에 반비례하다. • 전리도는 물질의 농도에 따라 변하므로 고유한 특성이 아니다. • 전리도는 온도, 전기전도도, 어는점내림에 비례하다. |
|
|
2-1. pH 측정기로 측정되는 값 |
(○) pH = -log γ H+[H+] (×) pH = -log[H+] (×) pH = log[H+] (×) pH = -log AH+[H+] (×) pH = pKW - log[OH-] |
pH = pKW + log[OH-] |
|
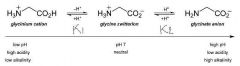
2-2. 아미노산의 등전점을 나타내는 [H+] |
(○) [H+] = √(K1•K2) (×) [H+] ≒ √(K1•C) (×) [H+] ≒ √(K2•C) (×) [H+] = √{(K1K2C+K1Kw) / (K1+C)} (×) [H+] = √(K1K2C+K1Kw) |
|
|
|
2-3. 완충용액의 pH를 나타내는 식 |
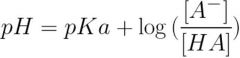
(○) 약산(HA) + 염(A-) : pH = pKa + log([A-]/[HA]) (○) 약염기(BOH) + 염(B+X-) : pOH = pKb + log([B+]/[BOH]) ⇒ pH = 14 - pOH (○) 약염기(B) + 짝산(BH+) : pH = pKa + log([B]/[BH+]) (○) 산(H2A) + 염(HA-) : pH = pK1 + log([HA-]/[H2A]) (×) 약산(HA) + 염(A-) : pH = pKa + log([HA]/[A-]) |
|
|
|
2-4. HA와 A-로 이루어진 완충액에 강산을 ΔC만큼 첨가하였을 때, 완충용액의 pH를 나타내는 식 |
(○) pH = pKa + log{([A-]-ΔC) / ([HA]+ΔC)} (×) pH = pKa + log([A-] / [HA])로 변화 없음 (×) pH = pKa + log{([A-]+ΔC) / ([HA]-ΔC)} (×) pH = pKa + log{([A-]-ΔC) / ([HA]-ΔC)} (×) pH = pKa + log{([HA]+ΔC) / ([A-]-ΔC)} |
• 강산을 HB라고 한다면, 강산은 해리도가 매우 높기 때문에 [HB] ↔ [H+] + [B-] 식에서 H+가 거의 ΔC만큼 생성된다. • 완충액의 산은 약산 HA이다. [HA] ↔ [H+] + [A-] 식에서 HA가 잘 생성된다. 여기에 첨가된 강산에서 ΔC만큼 H+가 생성되어도 바로 ΔC만큼 A-와 결합하여, ΔC만큼 AH가 생성된다([A-]-ΔC, [HA]+ΔC). |
|
|
2-5. 1M NH4Cl 용액의 [H+]에 가장 가까운 값은? 단, NH4OH : Kb = 1.0×10^-5, Kw = 1.0×10^-14 |
답 : 1.0 × 10^-5M • NH4+의 Ka = Kw / Kb = (1.0×10^-14) / (1.0×10^-5) = 1.0×10^-9 • 1M NH4+의 [H+]≒√(Ka•C) = √(1.0×10^-9 × 0.1) = 1.0×10^-5M |
|
|
|
2-6. 완충용액 중의 pH를 9.24가 되게 하려면 NH4OH와 NH4Cl의 농도비를 어떻게 조절해야 하는가? 단, NH4+의 pKa = 9.24 |
(○) 1 : 1 (×) 1 : 2 (×) 2 : 1 (×) 1 : 1.8 (×) 1.8 : 1 |
pH = pKa + log([NH4OH]/[NH4+]) pH = pKa = 9.24 ⇒ [NH4OH] = [NH4+] |
|
|
2-7. 아미노산 glutamic acid (H3A)는 분자 내 2개의 -COOH를 가지고 있다. 이 아미노산의 pK1 = 2, pK2 = 4, pK3 = 10 이라면 아미노산이 전하를 가장 적게 띠는 pH는? |
답 : pH = 3 H3A+ ↔ H2A ↔ HA- ↔ A-- pH = 2에서는 H3A+와 H2A가 반반 정도로 존재한다. pH = 3에서는 대부분이 H2A의 형태로 존재한다. pH = 4에서는 H2A와 HA-가 반반 정도로 존재한다. pH = 7에서는 대부분이 HA-의 형태로 존재한다. pH = 10에서는 HA-와 A--가 반반 정도로 존재한다. |
|
|
|
2-8. pH 7.2를 만들기 위하여 phosphate buffer를 사용한다. 적합한 완충용액의 구성은? 단, H3PO4의 pKa1 = 2.1, pKa2 = 7.2, pKa3 = 12.3 |
(○) 0.01M NaH2PO4와 Na2HPO4가 1 : 1로 섞인 용액 (×) 0.01M NaH2PO4와 Na2HPO4가 1 : 10으로 섞인 용액 (×) 0.01M Na2HPO4와 Na3PO4가 1 : 1로 섞인 용액 (×) 0.01M Na2HPO4와 Na3PO4가 1 : 10으로 섞인 용액 (×) 0.01M H3PO4와 NaH2PO4가 1 : 1로 섞인 용액 |
|
|
|
2-9. ☆ 등전점 (isoelectric point) |
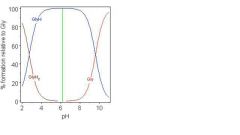
(○) 분자의 평균 전하가 0이 된다. (×) 등전점에서 물에 대한 용해도가 좋아진다. (○) 등전점에 있늘 물질을 전기장에서 움직이지 않는다. (×) 다양성자성 약산 1M 수용액의 pH이다. |
약산 1M 수용액의 pH는 0.5pKa이다. 농도 C인 약산의 수용액에서 C ≫ [H+] ≫ [OH-] ⇒ [H+] ≒ √(Ka•C) C = 1M ⇒ [H+] ≒ √Ka pH = -log [H+] ≒ -0.5log(Ka) = 0.5pKa |
|
|
2-10. 다음 화합물 중 염기도가 가장 큰 것은? |
C6H5ONa (C6H5OH : Ka = 1.1×10^-10) ∨ C3H7COONa (C3H7COOH : Ka = 1.5×10^-5) ∨ CH3COONa (CH3COOH : Ka = 1.8×10^-5) ∨ HCOONa (HCOOH : Ka = 1.8×10^-4) ∨ NaNO2 (HNO2 : Ka = 7.1×10^-4) |
Kb = Kw / Ka Kb ∝ 1/Ka |
|
|
2-11. 양성자성 용매 (protic solvent) |
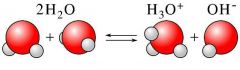
(×) 킬레이트 효과 (chelate effect) (○) 자기해리 (자체이온화, autoprotolysis) (×) 가리움 효과 (masking effect) (○) 수평화 효과 (leveling effect) |
• 킬레이트(chelate): 하나의 배위자가 중심 금속 원소와 두 곳 이상에서 결합하여 생성된 환상의 착화합물 • 가리움 효과(masking effect): 여러 성분이 공존하는 계에서 방해가 되는 성분을 착화합물로 만들어 분석에 방해가 되지 않도록 하는 것 • 물의 수평화 효과 (leveling effect): 물과 반응하는 아무리 강한 산이라도 H+(aq) 이온을 생성하고, 아무리 강한 염기라도 OH-(aq) 이온을 생성한다. |
|
|
2-12. 완충용량이 큰 pH 7.40의 완충 용액을 만들려면 다음 중 어느 화합물 용액에 NaOH를 가하는 것이 적절한가? |
(○) H3PO4 (pK1 = 2.15, pK2 = 7.20) (×) HAc (pKa = 4.76) (×) HCOOH (pKa = 3.75) (×) H2CO3 (pK1 = 6.35, pK2 = 10.33) (×) HF (pKa = 3.17) |
H3PO4는 pH = 7.20 에서 H2PO4-와 HPO4--가 반반씩 존재한다. |
|
|
2-13. 강전해질 |
(×) CH3NH2 (○) KOH (○) CaCl2 (○) (CH3)4NCl (○) Na2HPO4 |
|
|
|
2-14. 다음 중 0.05M phosphate buffer (pH = 7.2) 용액 1L를 만들기에 적합한 시약은? 단, H3PO4 pK1 = 2.1, pK2 = 7.2, pK3 = 12.1 |
(○) NaH2PO4 0.025mol과 Na2HPO4 0.025mol (×) H3PO4 0.025mol과 NaH2PO4 0.05mol (×) Na2HPO4 0.025mol과 Na3PO4 0.025mol (×) NaH2PO4 0.05mol과 Na2HPO4 0.05mol (×) Na2HPO4 0.05mol과 Na3PO4 0.05mol |
|
|
|
2-15. 0.1M NaHA 수용액의 pH 값은? 단, H2A의 pK1 = 7.0, pK2 = 11.0 |
답 : pH=9 HA-의 pH는 pK1과 pK2의 평균치에 가깝다. |
|
|
|
2-16. 다양성자성산의 등전점 |
(○) 다양성자성산이 띠고 있는 전하의 평균이 0이 되는 점이다. (○) 일반적으로 등전점에서 용해도가 가장 낮다. (○) 이양성자성 약산의 경우 등전점의 pH는 pK1과 pK2의 평균치이다. (×) 등전점에 있는 다양성자성산은 전기장에서 전극 쪽으로 잘 이동한다. |
등전점에 있는 다양성자성산은 전기적으로 중성이므로 전기장에서 움직이지 않는다. |
|
|
2-17. 0.1M H2A 수용액 중에 존재하는 [A--]의 농도는? 단, H2A의 K1 = 10^-7, K2 = 10^-15 |
답 : 10^-15 이양성자성 약산의 수용액에서 [A--] = K2 |
|
|
|
3-1. 용해도곱 Ksp가 9×10^-12인 염 BA의 포화용액 중의 [B+]의 농도는? |
답 : 3×10^-6 [A-]=[B+] Ksp = [A-][B+] = [B+][B+] [B+] = √(Ksp) |
|
|
|
3-2. 용해도곱 (solubility product) |
(○) 일정한 온도, 압력하에서 난용성염의 포화용액 중의 +, - 이온의 몰농도의 곱 (×) 일정한 온도, 압력하에서 난용성염의 포화농도의 제곱 (×) 일정한 온도, 압력하에서 용액 중 두 이온의 농도의 곱 (×) 일정한 온도에서 포화용액 중 두 이온의 농도의 곱 (×) 일정한 용액에 포함되어 있는 전체 이온의 농도의 곱 |
|
|
|
3-3. B2A와 같을 염의 침전이 형성되기 위한 조건을 올바르게 표현한 것은? 단, Ksp는 B2A의 용해도곱 |
(○) [B+]²[A--] > Ksp (×) [B+]²2[A--] < Ksp (×) [B+][A--] < Ksp (×) 2[B+][A--] > Ksp (×) 2[B+]²[A--] > Ksp |
|
|
|
3-4. Ag2CrO4의 포화 용액 중의 [Ag+]의 농도는? 단, Ag2CrO4의 Ksp=4×10^-12 |
답 : 2×10^-4M • [CrO4--]=[Ag+]/2 • Ksp = [Ag+]²[CrO4--] = [Ag+]²[Ag+]/2 [Ag+]³ = 2Ksp |
|
|
|
3-5. [CrO4--] = 1×10^-4M 용액이 있다. 여기에 AgNO3를 서서히 가하여 Ag2CrO4 침전이 막 생성되기 시작할 때의 [Ag+]는 얼마인가? 단, Ag2CrO4 Ksp=4×10^-12이고 용액의 부피 변화는 없는 것으로 간주한다. |
답 : 2×10^-4M 이상 Ksp = [Ag+]²[CrO4--] [Ag+] = √(Ksp/[CrO4--]) |
|
|
|
3-6. AgCl과 AgBr로 포함되어 있는 용액 내의 [Cl-] : [Br-]는? 단, AgCl Ksp=1×10^-10, AgBr Ksp=1×10^-13 |
답 : 1000:1 • AgCl Ksp=[Ag+][Cl-], AgBr Ksp =[Ag+][Br-] • [Cl-] = AgCl Ksp / [Ag+], [Br-] = AgBr Ksp / [Ag+] • [Cl-] : [Br-] = AgCl Ksp : AgBr Ksp |
|
|
|
3-7. Ag2CrO4 포화용액 중에 AgNO3 용액을 첨가하면 용액 중 CrO4--의 농도가 감소된다. 이 현상을 설명할 수 있는 것은? |
(○) 공통이온의 영향 (×) 염류 효과 (×) 염석 (×) 분별침전 (×) 용해도곱 감소현상 |
염류 효과는 액상 반응계에서, 염류를 첨가하였을 때 반응속도에 변화가 생기는 것을 말한다. 염석은 수용액에 다른 물질(주로 무기 염류)을 첨가하여 먼저 녹아 있던 물질을 석출시키는 것을 말한다. 분별침전은 두 종류 이상의 성분을 함유하는 용액에 침전시약을 가하여, 용해도의 차를 이용해서 두 종류 이상의 침전을 분리시키는 것이다. |
|
|
4-1. 착화합물 배위기의 성질 |
(○) 루이스 염기 (×) 빈 전자각 (○) 비공유 전자쌍 (×) 주로 1족, 2족 원소 |
배위자- 전자쌍 주개, 비공유 전자쌍, 루이스 염기 중심금속- 전자쌍 받개, 빈 전자각, 루이스 산 |
|
|
4-2. [Ag(NH3)2]+가 0.05M인 용액에 과잉의 NH3를 넣어 그 농도가 5M이 된 용액 중의 [Ag+]은? 단, [Ag(NH3)2]+의 생성상수 Kf는 1.5×10^7이다. |
답 : 1.3×10^-10 • Kf = [Ag(NH3)2+] / [Ag+][NH3]² [Ag(NH3)2+] = Kf [Ag+][NH3]² Kf 값이 매우 커서 처음 대부분이 [Ag(NH3)2+]=0.05M이다. • 여기에 과잉의 NH3를 넣어도 아주 소량의 착이온이 증가할 뿐이지 여전히 [Ag(NH3)2+]≒0.05M이다. • [Ag+] = [Ag(NH3)2+] / (Kf [NH3]²) ≒0.05 / (1.5×10^7 × 5²) = 1.3×10^-10M |
|
|
|
4-3. 10^-4M AgCl을 용해시키기 위한 NH3의 최소 농도는? 단, AgCl Ksp=10^-10, Ag(NH3)2+ Kf=10^8 |
답 : 1.0×10^-3M • 현재 [AgCl]=10^-4M은 거의 용해되지 못하고 대부분 침전물 상태이다. 여기에 NH3를 적당량 투입해서 [Ag+]=10^-4M와 결합시켜서 착이온으로 용해시키는 것이 목표다. • 착이온 형성해서 목표한 용해상태에는 [Ag(NH3)2+]=10^-4M, [Cl-]=10^-4M, [Ag+]=? 가 있다. • Ksp = [Ag+][Cl-] [Ag+] = Ksp / [Cl-] = 10^-10 / 10^-4 = 10^-6M • Kf = [Ag(NH3)2+] / [Ag+][NH3]² [NH3]² = [Ag(NH3)2+] / (Kf [Ag+]) = 10^-4 / (10^8 × 10^-6) = 10^-6M |
|
|
|
4-4. 10^-3M Zn++ 용액 1L에 고체 KCN 1mol을 가하였을 때 용액 중에 존재하는 [Zn++]를 구하여라. 단, Zn(CN)4-- Kf=1×10^18 |
답 : 1.0×10^-21M • Kf가 매우 커서 대부분이 착이온이다. [Zn(CN)4--]≒10^-3M, [CN-]=1M • Kf = [Zn(CN)4--] / [Zn++][CN-]⁴ [Zn++] = [Zn(CN)4--] / (Kf [CN-]⁴) = 10^-3 / (1×10^18 × 1⁴) = 1.0×10^-21M |
|
|
|
4-5. AgCl과 Hg2Cl2의 혼합물을 분리시킬 수 있는 것은? |
(○) NH4OH (×) 온수 (×) NaOH (×) HNO3 (×) H2SO4 |
AgCl은 Ag(NH3)2+ 착이온을 형성하여 용해됨 |
|
4-6. 4-7. ☆ 킬레이트의 안정성 |
(○) 킬레이트는 5원환이 가장 안정한데 이는 입체장애가 가장 적은 구조이기 때문이다. (×) 배위자의 산성이 강할수록 킬레이트는 안정하다. (×) 킬레이트 시약에 있는 다른 작용기는 킬레이트 화합물의 용해성과 관련 없다. (×) 한 금속이온에 단좌 배위자 여러 개가 결합하는 것이 다좌 배위자 소수가 결합되는 것보다 안정하다. (×) 킬레이트 환 내에 공명이 가능한 공액이중결합이 있으면 쉽게 분해된다. |
• 배위자의 염기성이 강할수록 킬레이트는 안정하다. • 킬레이트 시약에 있는 다른 작용기는 킬레이트 화합물의 용해성과 직접적인 관련이 있다. • 배위자의 배위기가 많아 중심 금속과 여러 자리에서 결합할수록 킬레이트는 안정하다. • 킬레이트 환 내에 공명이 가능한 공액이중결합이 있으면 더 안정하다. |
|
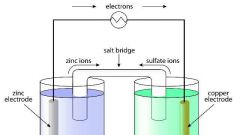
5-1. ☆ 갈바니 전지 |
(○) 두 개의 반쪽 전지를 연결한다. (○) 염다리가 필요하다. (○) 산화전극은 음극이 된다. (○) 전기화학적 전지이다. (×) 전극 전위의 절대값을 측정할 수 있다. (×) '||'는 염다리이고 전위차가 나타난다. |
전극 전위의 절대값을 측정할 수 없고, 다른 전극과의 차이를 측정할 수 있다. '||'는 염다리이고 전위차는 없다. |
|
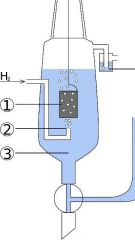
5-2. 표준수소전극을 표현한 식 |
(○) Pt | H2(g, 1atm) | H+(aq, A=1) (×) Ag | H+(aq, A=1) || H2(g, 1atm) (×) Pt | H+(aq, A=1) | H2(g, 1atm) (×) Pt | H2(g, 1atm) || H+(aq, A=1) (×) Ag | H2(g, 1atm) || H+(aq, A=1) |
|
|
|
5-3. ☆ 산화환원반응 |
(○) 산화반응과 환원반응은 동시에 진행된다. (○) 전극전위의 절대값은 측정할 수 없다. (×) 어떤 화학종이 전자를 얻으면 산화된다. (×) 금속의 환원전위는 금속이온의 농도와 무관하다. |
• 화학종이 전자를 얻으면 환원된다. • 전극전위의 절대값은 측정할 수 없고 단지 다른 전극과의 차이를 측정한다. • 각 금속의 표준환원전위는 일정하지만 환원전위는 용액 중 금속이온의 활동도에 따라 달라진다. |
|
|
5-4. 다음 반응의 표준전위(E°)는 얼마인가? 반응식: 2Ag+ + Zn(s) ↔ 2Ag(s) + Zn++ 단, Ag+ + e- ↔ Ag(s)의 E°=+0.80V, Zn++ + 2e- ↔ Zn(s)의 E°=-0.76V |
답 : +1.56V |
|
|
|
5-5. 다음 식으로 나타나는 전지의 알짜반응의 식과 기전력 E°cell을 옳게 기술하시오. 전지식: Zn | ZnSO4 || CuSO4 | Cu 단, Zn++ + 2e- ↔ Zn의 E°=-0.763V, Cu++ + 2e- ↔ Cu의 E°=+0.337V |
답 : Zn + CuSO4 ↔ Cu + ZnSO4, E°=+1.100V |
|
|
|
6-1. 실험오차 |
(○) 실험오차는 계통오차와 우연오차로 분류할 수 있다. (○) 계통오차(systematic error)는 determinate error라고도 부르며, 오차가 일어나는 원인을 추궁할 수 있다. (○) 우연오차(random error)는 indeterminate error라고도 부르며, 오차가 일어나는 원인을 추궁할 수 없다. (×) 공시험은 우연오차를 제거하는 방법이다. |
계통오차를 제거하는 시험법: 공시험(blank test), 조절시험(control test), 회수시험(recovery test), 맹시험(blind test), 평행시험(parallel test) |
|
|
6-2. a) 1.9030, b) 0.03910, c) 1.40×10⁴ |
(○) a)에는 5개의 유효숫자가 있다. (×) b)에는 6개의 유효숫자가 있다. (×) b)에는 5개의 유효숫자가 있다. (×) c)에는 2개의 유효숫자가 있다. |
b)에는 4개의 유효숫자가 있다. c)에는 3개의 유효숫자가 있다. |
|
|
6-3. 6-4. 유효숫자 계산 |
(○) 3.72 × 2.3 = 8.5 (○) 107.3 - 23.7 = 83.6 (○) (27.13 ÷ 13.60) × 3.21 = 6.40 (×) 1.023 + 3.71 = 4.733 (×) 13.1 - 2.78 = 10.32 (×) 5.74 ÷ 3.2 = 1.79 (×) (26.31 ÷ 2.72) + 3.1 = 12.77 |
• 1.023 + 3.71 = 4.73 • 13.1 - 2.78 = 10.3 • 5.74 ÷ 3.2 = 1.8 • (26.31 ÷ 2.72) + 3.1 = 12.8 |
|
|
6-5. 표준편차 |
(○) 표준편차(standard deviation)가 작을수록 정밀도가 높다. (○) 측정값들이 가우스 분포로 bell-shape 분포를 나타낼 때 평균값은 측정값들의 집중경향성을 나타내는 대표값이고 표준편차란 측정값들의 분포의 폭의 크기를 나타낸다. (○) 표준편차와 정확도는 상관이 없다. (×) 표준편차가 클수록 정확도가 낮다. |
표준편차가 클수록 정밀도가 낮다. |
|
|
6-7. 유효숫자의 자리수가 4인 것 |
(○) 1.001 × 10³ (×) 16,000 (×) 1.6 × 10⁴ (×) 5 × 10^-2 (×) 160,000 |
|
|
|
6-8 유효자리수가 3인 것 |
(○) 1000 - 2.5 (×) 1000 + 2.5 (×) 1000 × 2.5 (×) 1000 ÷ 2.5 (×) 1000 + 3.5 |
|
|
|
6-9. 곱셈 또는 나눗셈을 하여 얻을 값의 유효자리수 |
(○) 곱셈 또는 나눗셈에 참여한 값들의 유효자리수에 지배된다. (×) 끝자리수의 단위가 가장 작은 것에 지배된다. (×) 끝자리수의 단위가 가장 큰 것에 지배된다. (×) 유효자리수의 단위가 가장 작은 것에 지배된다. (×) 유효자리수의 단위가 가장 큰 것에 지배된다. |
|
|
|
6-10. 유효숫자의 기재 |
(○) 자리수보다 한자리 더 많이 기재하되 그 이하는 사사오입하여 기재한다. (×) 자리수만 기입하되 그 이하는 사사오입하여 기재한다. (×) 자리수만을 기재한다. (×) 자리수보다 한자리 더 많이 그대로 기재한다. (×) 자리수보다 두자리 더 많이 그대로 기재한다. |
|
|
|
6-11. 일어나는 원인을 추궁할 수 없는 오차 |
(○) 우연오차이며 정규분포한다. (×) 정오차이며 정규분포한다. (×) 부오차이며 정규분포한다. (×) 상대오차이며 부정규분포한다. (×) 절대오차이며 부정규분포한다. |
|
|
|
7-1. 0.055M-H2SO4 100mL를 중화시킬 수 있늘 0.1M-NaOH는 몇 mL? |
답 : 110mL • H2SO4≡2NaOH • 몰농도(M1)×부피(V1) = 몰농도(M2)×부피(V2) 2×0.055M×100mL = 0.1M×V2mL V2 = 110mL |
|
|
|
7-2. 10w/v% NaOH(m.w.=40)의 몰농도 |
답 : 2.5M • 몰농도(M) = 몰수(n) / 1L = 질량(m) ÷ 분자량(m.w.) / 1L = 용매부피(V) × 백분율 ÷ 분자량(m.w.) / 1L = 1L × (10kg/100L) ÷ 40g/mol / 1L × 1000g/1kg = 2.5mol/L |
|
|
|
7-3. Na2CO3(m.w.=106) 1.06g을 취하여 H2SO4 용액을 표정하니 10mL를 소비했다. H2SO4 용액의 몰농도는?(지시약 M.O.) |
답 : 1.000M • Na2CO3≡H2SO4 • 몰농도(M) = 몰수(n) / 부피(V) = 질량(m) ÷ 분자량(m.w.) / 부피(V) = 1.06g ÷ 106g/mol / 10mL × 1000mL/1L = 1mol/L |
|
|
|
7-4. 90% H2SO4(S.G.=1.82) 몇 mL를 취하여 H2O에 가해서 500mL로 하면 0.25M-H2SO4 용액이 된다. 단, H2SO4 m.w.=98.00 |
답 : 12.25×100 / 1.82×90 • 몰농도(M2)=0.25mol/L 부피(V2)=500mL=0.5L • 필요몰수(n필) = 몰농도(M2)×부피(V2) = 0.25mol/L× 0.5L = 0.125mol • 몰농도(M1)×부피(V1) = 필요몰수(n필) = 몰농도(M2)×부피(V2) • 부피(V1) = 필요몰수(n필) / 몰농도(M1) = 필요몰수(n필) / (몰수(n) / 원액1000mL) = 필요몰수(n필) / (질량(m)÷분자량(m.w.) / 원액1000mL) = 필요몰수(n필) / (원액1000mL×비중(S.G.)×백분율(P)/100÷분자량(m.w.) / 원액1000mL) = 필요몰수(n필)×분자량(m.w.)×100 / (백분율(P)×비중(S.G.)) = 0.125mol×98.00g/mol×100 / (90%×1.82g/mL) = 12.25×100 / (1.82×90)mL |
|
|
|
7-5. H2SO4 용액 15mL를 취하여 M-NaOH으로 표정하니 31.38mL를 소비했다. H2SO4의 농도는 ( )M이다. |
답 : 1.046M • H2SO4≡2NaOH • 몰농도(M1)×부피(V1) = 몰농도(M2)×부피(V2) M1 = M2 × V2 / V1 = 1M × 31.38mL / 15mL = 2.092M • [H+]=2.092M이고 H2SO4는 2가이기 때문에 [H2SO4]=1.046M이다. |
|
|
|
7-6. NaOH(m.w.=40.00) 4.40g을 물에 녹여 250mL로 만든 용액의 몰농도 |
답 : 0.44M • 몰농도(M) = 몰수(n) / 부피(L) = 질량(m)÷분자량(m.w) / 부피(L) = 4.40g÷40.00g/mol / 0.25L = 0.44mol/L |
|
|
|
7-7. 0.1050M-HCl 30mL를 중화시키는데 NaOH 표준액 25mL를 소비하였다. 이 NaOH액의 몰농도는? |
답 : 0.1050×30/25M • HCl≡NaOH • M1=0.1050M, V1=30mL, V2=25mL • 몰농도(M1)×부피(V1) = 몰농도(M2)×부피(V2) M2 = M1 × V1 / V2 = 0.1050M × 30mL / 25mL |
|
|
|
7-8. 0.102M-NaOH 100mL에 물 400mL를 가했을 때 몰농도 |
답 : 0.0204M • M1=0.102M, V1=100mL, V2=400mL • 몰농도(M1)×부피(V1) = 몰농도(M2)×부피(V2) M2 = M1 × V1 / V2 = 0.102M × 100mL / 500mL = 0.0204M |
|
|
|
7-9. 1) 0.1M-NaOH 100mL 중에 함유되는 NaOH 밀리몰수 2) H2SO4(m.w.=98.00) 0.49g의 밀리몰수 |
1) 답 : 10mmol 몰수(n) = 몰농도(M) × 부피(V) = 0.1mmol/mL × 100mL = 10mmol 2) 답 : 5mmol 몰수(n) = 질량(m) ÷ 분자량(m.w) = 0.49g ÷ 98.00g/mol × 1000mmol/1mol = 5mmol |
|
|
|
8-1. HAc를 0.1M-NaOH로 적정할 때 적당한 지시약 |
(○) PP (○) TP (×) BCG (×) MR (×) MO (×) PR |
|
|
|
8-2. 약산을 강염기 표준액으로 적정 |
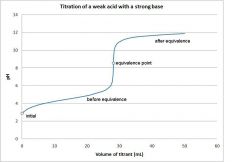
|
|
|
|
8-3. 산 표준액을 표정하려고 한다. 다음 중 가장 적당한 표준물질은? |
(○) Na2CO3 (○) KHCO3 (×) K2Cr2O7 (×) As2O3 (×) Na2SO4 (×) KHP (potassium hydrogen phthalate) |
|
|
|
8-4. 알칼리 표준액을 표정하려고 한다. 다음 중 가장 적당한 표준물질은? |
(○) KHP (potassium hydrogen phthalate) (○) NaSO3NH2 (○) H2C2O4 (○) HCl (×) NH2HSO4 (×) Na2C2O4 (×) KHCO3 (×) Na2S2O3 |
|
|
|
8-5. KHCO3를 사용하여 0.1M-HCl을 표정하려고 한다. 다음 지시약 중 가장 적당한 것은? |
(○) MR (○) MO (×) BTB (×) BCG (×) PP (×) TP |
|
|
|
8-6. H3PO4 + H2SO4 혼합액에 MO를 넣고 0.1M-NaOH 액으로 적정하여 a mL를 소비하였다. 다시 동량의 시료에 PP를 넣고 0.1M-NaOH 액으로 적정하여 b mL를 소비하였다. |
(○) H3PO4 ⅓량 중화하는데 (b-a) mL 소비 (×) H3PO4 ⅔량 중화하는데 (b-a) mL 소비 (×) H3PO4 전량 중화하는데 b-(b-a) mL 소비 (×) H3PO4 ⅔량 중화하는데 3(b-a) mL 소비 (×) H3PO4 ½량 중화하는데 b-(b-a) mL 소비 |
|
|
|
8-7. Warder 법으로 NaOH + Na2CO3 혼합액을 적정하였을 때 각 지시약에 대한 M-HCl 소비량은 <다음>과 같다. 검액 중 NaOH와 반응한 M-HCl 양은? <다음> PP 25mL, MO 5mL |
답 : 20mL |
|
|
|
8-8. aspirin (m.w.=180) 시료 S g을 취하여 0.1M-NaOH 50mL를 넣고 가온 후 0.05M-H2SO4으로 역적정하여 a mL를 소비하였다. 따로 공시험한 결과 0.05M-H2SO4 b mL가 소비되었다. S g 중의 aspirin의 g 수는? |
답 : 0.09 × (b-a) aspirin 180g≡2M-NaOH 1L≡1M-H2SO4 1L aspirin 90g≡1M-NaOH 1L≡0.5M-H2SO4 1L aspirin 0.009g≡0.1M-NaOH 1mL≡0.05M-H2SO4 1mL ?? |
|
|
|
8-9. NaOH 표준액을 조제할 때 일단 끓여서 식힌 물을 사용하는 이유 |
(○) 적정할 때 탄산오차를 적게 하기 위하여 (×) 조제할 때 용해도를 높이기 위하여 (×) 용존 산소를 제거하기 위하여 (×) 적정할 때 중화반응을 촉진시키기 위하여 (×) 소독하기 위하여 |
|
|
|
8-10. 0.5M-HCl을 KHCO3를 기본물질로 하여 표정할 때 적당한 지시약 |
(○) MR (○) MO (×) PR (×) PP (×) TP (×) BCG |
|
|
|
9-1. 프탈산수소칼륨(표준물질, m.w.=204.23) 500.0mg을 빙초산 80mL에 녹여 0.1M-HClO4(m.w.=100.47)로 적정했을 때 24.13mL를 소비하였다. 공시험에 0.05mL 소비하였다면 이 0.1M-HClO4의 몰 농도계수(factor)는 얼마인가? |
답 : 1.017 • 표준물질(a)=500.0mg=0.5g, 실제값(V)=(24.13-0.05)mL • KHP 204.23g≡M-HClO4 1000mL KHP 20.423g≡0.1M-HClO4 1000mL KHP a g≡ 0.1M-HClO4 V0 mL V0 = 1000 × a ÷ 20.423 mL • f = V0 / V = 1000 × a ÷ 20.423 / V = 1000 × 0.5 ÷ 20.423 / 24.08 = 1.017 |
|
|
|
9-2. Karl Fischer 수분측정법 |
(○) Karl Fischer 법은 비수용매 중에서의 산화환원 반응을 이용한 수분적정법이다. (○) 시액은 수분과 정량적으로 반응한다. (○) 시액의 factor는 시액 1mL에 대응하는 물의 mg 수로 표시한다. (○) Karl Fischer 법으로 결정수의 정량도 가능하다. |
|
|
|
9-3. Karl Fischer 시액을 표정하기 위하여 주석산나트륨을 102.2mg 달았다면 몇 mg의 물을 취한 셈인가? 단, 주석산나트륨 C4H4O6Na2•2H2O, C:12.011, H:1.008, O:15.999, Na:22.990 |
답 : 16.0mg • C4H4O6Na2•2H2O 분자량 = 12.011×4 + 1.008×8 + 15.999×8 + 22.990×2 = 230.08 • 2H2O 분자량 = 1.008×4 + 15.999×2= 36.03 • 주석산나트륨 : 물 = 230.08 : 36.03 = 102.2 mg : x mg x = 16.0mg |
|
|
|
9-4. 비수용매 |
(○) 프로톤 용매는 프로톤과의 결합력에 따라 산성, 염기성, 양성용매의 3 가지로 구분한다. (○) 비프로톤 용매는 수평화 효과를 갖지 않는다. (○) 혼합 용매는 프로톤 용매와 비프로톤 용매의 장점을 이용하기 위해 두 가지를 섞은 것이다. (○) 카르복실산은 산성용매의 대표이다. (×) 비프로톤 용매는 용매 분자내에 수소원자가 없다. |
|
|
|
9-5. 다음에 기술된 내용은 카페인 (C8H10N4O2, m.w.=194.19)의 비수적정법에 관한 것이다. [ ]에 들어가야 할 수치는? "이 약을 80℃에서 4 시간 건조하고 그 약 0.4g을 정밀히 달아, 무수초산빙초산 혼액(6:1) 70mL를 가하여 녹이고, 0.1M 과염소산으로 적정한다 (지시약: 염화메틸로자닐린 시액 3 방울). 단, 적정의 종말점은 액의 자색이 녹색을 거쳐 황색으로 변할 때로 한다. 같은 방법으로 공시험을 하여 보정한다. 0.1M 과염소산 1mL = [ ]mg" |
답 : 19.419 |
|
|
|
9-6. 0.1M-HClO4 표준액 1000mL를 조제하려면 과염소산(m.w.=100.47, S.G.=1.664, 71%)을 ( )mL를 취하여 빙초산 800mL가 들어있는 volumetric flask에 넣는다. 계속하여 무수초산 30mL를 가한 후 빙초산을 더 가하여 1000mL로 한다. ( )의 답은? |
답 : 약 8.7mL 필요부피(V) = 몰수(n)×분자량(m.w.)×100 / (백분율(P)×비중(S)) = 0.1mol×100.47g/mol×100 / (71%×1.664g/mL) = 8.5mL |
|
|
|
9-7. 0.1M-HClO4 표준액을 표정하는데 가장 적합한 표준물질 |
(○) 프탈산수소칼륨 (KHP) (×) As2O3 (×) phenol (×) benzoic acid (×) NaCl |
|
|
|
9-8. 0.1M-HClO4 표준액을 표정하는데 가장 적합한 지시약 |
(○) crystal violet (CV) (×) phenolphthalein (×) thymol blue (×) eosine (×) fluorescein |
|
|
|
9-9. caffeine을 0.1M-HClO4 표준액으로 적정할 때 가장 적합한 용매 |
(○) 무수초산-빙초산-혼합액 (×) 증류수 (×) benzene (×) ethanol (×) DMF |
|
|
|
9-10. 구연산 피페라진(piperazine citrates, m.w.=642.66) 1mole은 HClO4 몇 mole에 해당하는가? |
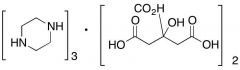
답 : 6 mole |
(piperazine)3(citrate)2 형태로 존재하는데, piperazine에 N이 2개. 총6개의 N이 H+와 반응할 수 있으므로 6mole. |
|
|
10-1. 0.1mol/L-AgNO3 액을 표정할 수 있는 일차 표준물질 |
(○) NaCl (×) KHCO3 (×) NH4SCN (×) Fe (×) Sn |
|
|
|
10-2. 차광 보존을 요하는 것 |
(○) 0.1mol/L-AgNO3 (×) 0.1mol/L-K2Cr2O7 (×) 0.1mol/L-Ba(OH)2 (×) 0.1mol/L-H2SO4 (×) 0.1mol/L-NaCl |
|
|
|
10-3. Cl-을 0.1M AgNO3로 적정할 때 흡착지시약 |
(○) fluorescein (×) diphenylamine (×) phenolphthalein (×) eosin (×) K3Fe(CN)6 |
|
|
|
10-4. NaCl을 Volhard 간접법으로 정량할 때 발생하는 부반응의 방지를 위해 AgCl 침전에 엷은 막을 입혀 NH4SCN과 작용하지 못하도록 하기 위해 가하는 물질 |
(○) nitrobenzene (×) diazomethane (×) acetone (×) KHCO3 (×) H2S |
|
|
|
10-5. 시료 - 정량법 |
(○) 요오드팅크 중 I2 - Na2S2O3 법 (iodimetry) (○) KBr - Fajans 법 (○) KI + KCl 중 KI - Kolthoff 요오드 전분법 (○) KCl - Mohr 법 (×) 표백분 중 유효염소 - Volhard 법 |
표백분 중 유효염소 - Iodometry(간접요오드 적정법) Na2S2O3
|
|
|
10-6. KCN을 0.1mol/L-AgNO3로 Ag[Ag(CN)2]의 백색 침전이 생기기 시작하는 점까지 적정하였다. 0.1mol/L-AgNO3 1mL≡( )mg KCN (m.w.=65.11) |
답 : 13.022mg AgNO3 + 2KCN → Ag[Ag(CN)2]↓ 1mol/L-AgNO3 1mL≡130.22mg KCN |
|
|
|
11-1. EDTA로 적정하기 전에 금속이온을 함유하는 용액에 완충액을 가하는 이유 |
(○) 금속이온이 수산화물로 침전하는 것을 방지하기 위하여 (○) 금속지시약이 일장한 pH 범위에서만 변색하므로 (○) 조건상수값이 pH에 따라 변하므로 (×) 금속의 산화를 방지하기 위하여 |
|
|
|
11-2. 킬레이트 적정에 미치는 인자 |
(○) 적정액의 pH (○) 금속이온의 가수분해 (○) 경쟁 리간드의 농도 (○) 킬레이트의 안정도 상수 |
|
|
|
11-3. pH 12에서 0.1M-MgCl2 100mL를 0.1M-EDTA로 적정시 당량점에서의 [Mg²+]를 구하여라.(생성상수=5.0×10^8) |
답 : 10^-5M • 처음 농도(C)에 적정액만큼 부피가 추가되서 농도/2가 된다. [MY]=C/2 • 당량점 KMY = [MY] / [M][Y] = [MY] / [M]² [M]² = C/(2KMY) • [M] = √(C/(2KMY)) = √(0.1/(2×5.0×10^8)) = 10^-5M |
|
|
|
11-4. 건조 수산화알루미늄겔 시료에 염산을 넣어 가열하고, 그 일부에 0.01M-EDTA를 과량 가한 후 pH 4.8에서 0.05M 초산아연액으로 역적정하였다. 0.01M-EDTA 1mL에 해당하는 시료 중의 Al2O3(m.w.=102)의 mg 수는? |
답 : 0.51mg Al2O3 + 2EDTA → 2[Al(EDTA)]+ 2M-EDTA 1mL≡102mg Al2O3 1M-EDTA 1mL≡51mg Al2O3 |
|
|
|
11-5. 금속이온의 선택적정에 이용되는 방법 |
(○) pH의 조절에 의한 방법 (○) Masking에 의한 방법 (○) 침전 및 추출에 의한 방법 (×) 농축에 의한 방법 |
|
|
|
11-6. 0.05mol/L-EDTA 액을 만들어 다음과 같이 표정하였다. 0.05mol/L-EDTA 액의 몰농도계수로서 가장 가까운 값은? 아연(표준시약, Zn=65.39) 0.8320g을 달아 묽은 염산 12mL 및 브롬수 5 방울을 넣어 천천히 가온해서 녹인 다음, 끓여서 과량의 브롬을 제거한 다음 물을 넣어 정확히 200mL로 한다. 이 액 20mL를 정확히 취하여 수산화나트륨용액(1→50)을 넣어 중화한 다음 pH 10.7의 암모니아•염화암모늄 완충액 5mL 및 EBT•NaCl 지시약 40mg을 넣고 조제한 0.05 mol/L-EDTA액으로 적정하였더니 25.20mL가 소비되었다. |
답 : 1.010 • 질량=0.8320g, 분자량=65.39g/mol, 부피=200mL=0.2L, 사용 부피=20mL • 아연 몰농도(M') = 몰수(n) / 부피(V) = 질량(m)÷분자량(m.w.) / 부피(V) = 0.8320g÷65.39g/mol / 0.2L • 1M-Zn 1mL≡1M-EDTA 1mL • f = M'V' / MV = 0.8320g÷65.39g/mol/0.2L×20mL / (0.05M×25.20mL) = 1.010 |
|
|
|
12-1. 과망간산적정법 |
(○) 일정량의 시료 용액에 H2SO4을 충분히 가하여 산성으로 한 후 적정한다. (○) 당량점을 지나 과잉의 MnO4-에 의한 연한 홍색이 나타날 때가 종말점이다. (○) 온도가 80도를 넘으면 MnO4-이 분해된다. (○) KMnO4 표준용액은 갈색유리병에 넣어 어두운 곳에 보관한다. |
|
|
|
12-2. KMnO4 표준액을 표정할 때 쓰이는 일차표준물질 |
(○) Na2C2O4 (×) K2Cr2O7 (×) Na2S2O3•5H2O (×) NaHCO3 (×) Fe2(SO4)3 |
|
|
|
12-3. 0.1M-KMnO4 1000mL는 H2O2(m.w.=34.01) 몇 g을 산화시킬 수 있는가? |
답 : 8.503g 2KMnO4≡5H2O2 KMnO4≡5/2H2O2 1M-KMnO4 1000mL≡34.01g 5/2H2O2 |
|
|
|
12-4. 아스코르빈산 시료 0.2020을 칭취하여 메타인산 시액(1→50) 50mL에 녹이고 0.05M-I2 표준액으로 적정하여 22.00mL를 소비하였다. 아스코르빈산 정에 들어있는 L-ascorbic acid (C6H8O6, m.w.=176.16)의 함량%(w/w)를 구하시오. |
답 : 95.9% • I2≡C6H8O6 1M-I2 1mL≡176.16mg C6H8O6 0.05M-I2 1mL≡8.806mg C6H8O6 • 함량% = 측정량 ÷ 채취량 × 100 = 0.008806g-C6H8O6 / 1mL-I2 × 22.00mL-I2 ÷ 0.2020g-C6H8O6 × 100 = 95.9% |
|
|
|
12-5. 포비돈 요오드액 5.00mL를 정확하게 취하여 유리 마개 삼각플라스크에 넣고 물을 넣어 30mL로 한 다음 전분시액 3mL를 가하고 0.02M 티오황산나트륨으로 적정하여 20.00mL를 소비하였다. 포비돈 요오드액 중 요오드(I, m.w.=127)의 함량%(w/v)를 구하시오. |
답 : 1.02% • Na2S2O3≡I 1M-Na2S2O3 1mL≡127mg-I 0.02M-Na2S2O3 1mL≡0.00254mg-I • 함량% = 측정량 ÷ 채취량 × 100 = 0.00254mg-I / 1mL-Na2S2O3 × 20mL-Na2S2O3 ÷ 5.00mL-I × 100 = 1.02%(mg/mL) |
|
|
|
12-6. 요오드 적정에 사용되는 I2 표준액 |
(○) I2는 물에 녹기 어려우므로 KI을 가하여 용해도를 증가시킨다. (○) 산성에서는 I-이 공기 또는 용액 중의 산소에 의해 산화되어 I2를 생성한다. (○) 알칼리성에서는 I2는 불균형반응이 진행되어 IO- 또는 IO3-을 생성한다. (○) I2 표준액으로 적정할 때는 pH 5~9 범위가 적당하다. |
|
|
|
12-7. CaOCl2 중 유효염소의 정량은 A와 B를 가하여 유리되는 C를 D 표준액으로 적정하면 된다. A-B-C-D에 적합한 답은? |
(○) HCl - KI - I2 - Na2S2O3 (×) NaOH - KI - I2 - Na2S2O3 (×) NaHCO3 - H2O2 - NaI - AgNO3 (×) HCl - IBr - HBr - AgNO3 (×) NH4Cl - NaOH - NH3 - H2SO4 |
|
|
|
12-8. H2O2 (m.w.=34.01) 1mL에 d-H2SO4 10mL 및 KI 2g을 가하고 반응 후 0.1mol/L-Na2S2O3로 적정할 때 0.1mol/L-Na2S2O3 1mL ≡ ( )g H2O2에 대응한다. |
답 : 34.01/20000 2mol/L-Na2S2O3 1mL≡34.01mg H2O2 1mol/L-Na2S2O3 1mL≡34.01/2000g H2O2 |
|

