![]()
![]()
![]()
Use LEFT and RIGHT arrow keys to navigate between flashcards;
Use UP and DOWN arrow keys to flip the card;
H to show hint;
A reads text to speech;
7 Cards in this Set
- Front
- Back
- 3rd side (hint)
|
Fórmula da concentração comum |
C = Massa do soluto —----------------------------- Volume da solução |
|
|
|
Ao observar o rótulo de leite, nota-se que em cada 200ml de leite, há 9gde carboidratos. Qual a concentração em g/L de carboidrato no leite? |
C = ? m = 9g V = 200 ml = 0,2L
C = m/v C = 9/ 0,2 C = 45 g/L |
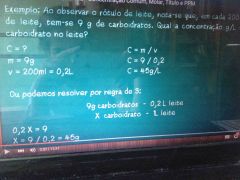
Ou, regra de 3 |
|
|
CUIDADO PARA NÃO CONFUNDIR CONCENTRAÇÃO COMUM COM DENSIDADE |
Concentração comum:
Massa soluto/ volume
Densidade:
Massa solução/ volume |
|
|
|
Fórmula de concentração molar (M) |
M = N de mols/ Volume
N de mols = massa do soluto/ MM (massa molar)
M = massa do soluto/ MM . Volume |
|
|
|
Qual é a molaridade de uma solução com volume de 250 ml que contém 55,5 g de cloreto de cálcio (CaCl2)? |
M = ? m = 55,5g V = 250ml = 0,25L MM = 11g/mol
M = m/ MM . V M = 55,5 / 111 . 0,25 M = 2 mol/L |
|
|
|
Fórmula de Título (T) |
T = m soluto/ m solução
T. 100= % |
|
|
|
Calcule o título e a porcentagem em massa de uma solução feita a partir da dissolução de 368g de glicerina, C3H8O3, em 1600g de água. |
T = ? m soluto = 368g m solução = 368 + 1600= 1968g
T= m soluto/ m solução T = 368 / 1968 T = 0,18
0,18 . 100= 18% |
|

